Atropoizomeria jest rodzajem stereochemii będącej konsekwencją utrudnienia swobody obrotu wokół wiązania łączącego układy aromatyczne. Wykazują ją odpowiednio podstawione biaryle i związki analogiczne. Rola atropoizomerii zarówno w chemii, jak i biologii została już dobrze udokumentowana. Wiele związków biologicznie czynnych występuje w postaci czystych atropoizomerów i zjawisko to ma ważne konsekwencje dla chemii medycznej.
Podczas naszej współpracy z Agencją Bezpieczeństwa Wewnętrznego dokonaliśmy syntezy wielu oligo-arylo podstawionych związków heterocyklicznych wykorzystując reakcję sprzęgania Suzuki-Miyaury.
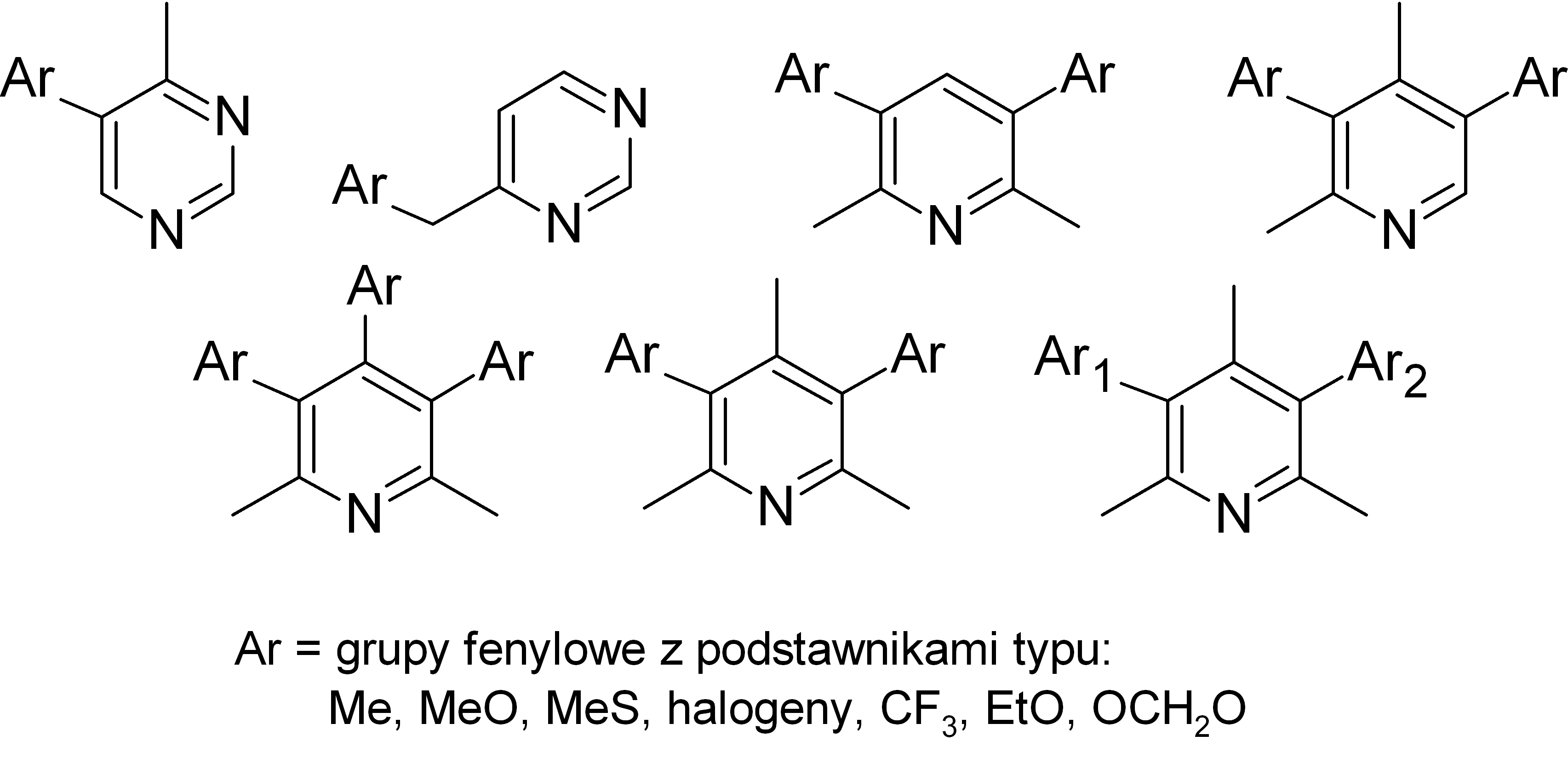
W niektórych przypadkach obserwuje się obecność stabilnych stereoizomerów pochodzących z obecności osi chiralnej.
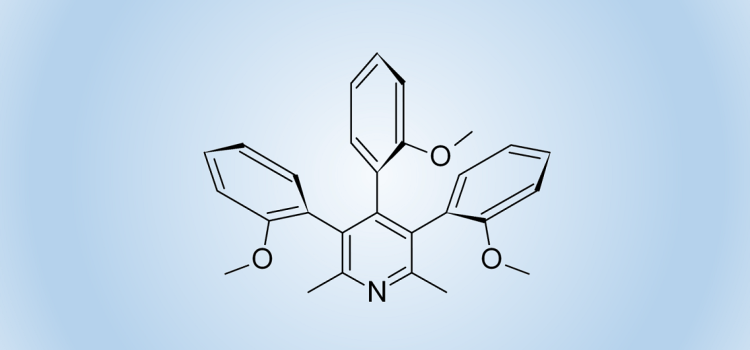
Na przykład okazało się, że reakcja Suzuki z tribromo-2,6-lutydyną i kwasem 2-metoksyfenyloborowym prowadzi do powstania 3,4,5-tri-(2-metoksyfenylo)-2,6-lutydyny w postaci mieszaniny trzech stabilnych w temperaturze pokojowej w diastereoizomerów. Każdy z nich wyizolowaliśmy i w pełni scharakteryzowaliśmy, w tym określiliśmy ich stereochemię na drodze strukturalnej analizy rentgenowskiej. Chiralny izomer anti-syn jest mieszaniną racemiczną, którą udało się rozdzielić na poszczególne enancjomery. Ich stereochemię absolutną również udało się określić. Badaliśmy także termiczną stabilność atropoizomerów za pomocą metod dynamicznych (NMR, HPLC), wspomaganych obliczeniami kwantowo-chemicznymi.
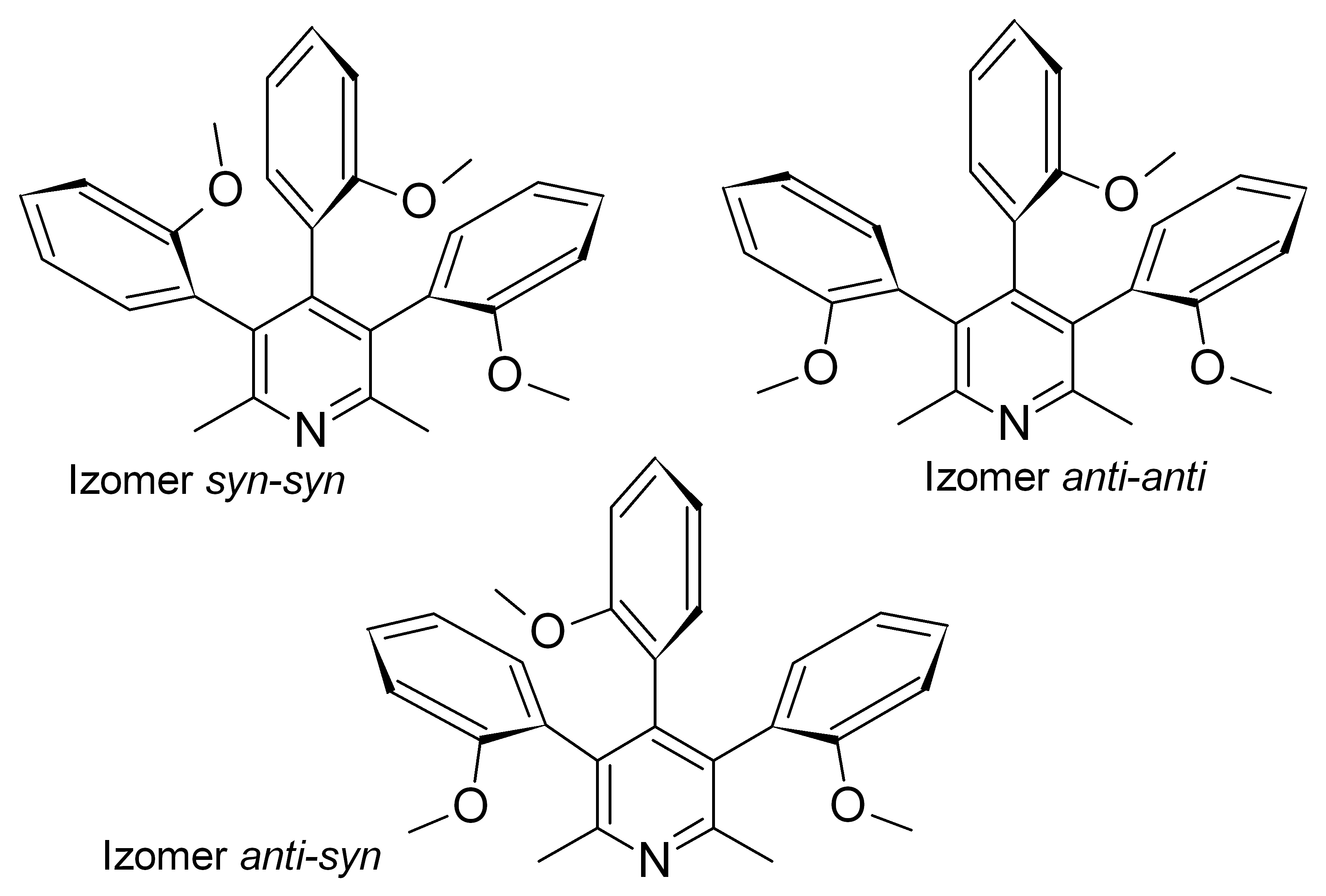
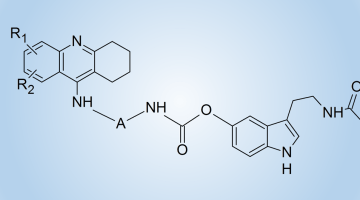
Zjawisko atropoizomerii zaobserwowaliśmy także w przypadku pochodnych 4-amino-2,6-lutydyny.
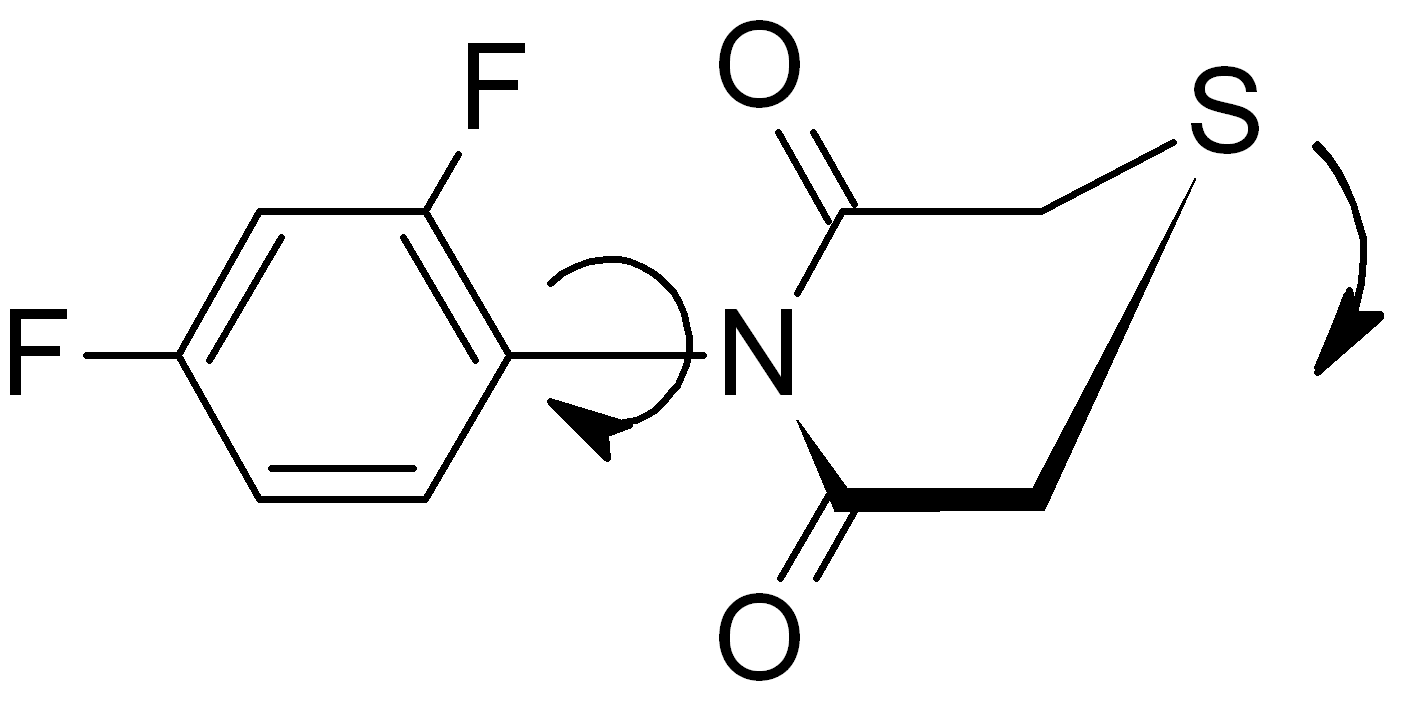
Dokonaliśmy również syntezy szeregu dotychczas nieznanych N-arylo-podstawionych pochodnych tiomorfolino-3,5-dionu. Gdy pierścień aromatyczny posiadał podstawnik w pozycji orto-, obserwowaliśmy tworzenie stabilnych w temperaturze pokojowej diastereoizomerów. Stereochemię dynamiczną tych związków badaliśmy metodami spektroskopowymi i obliczeniowymi.
Błachut D., Wojtasiewicz K., Krawczyk K., Maurin J.K., Szawkało J., Czarnocki Z., „Identification and synthesis of by-products found in 4-methylthioamphetamine (4-MTA) produced by the Leuckart method” Forensic Sci. Int. 216, 108-120 (2012)
Roszkowski P., Błachut D., Maurin J.K., Woźnica M., Frelek J., Pluciński F., Czarnocki Z., „Atropisomerism in 3,4,5-Tri-(2-methoxyphenyl)-2,6-lutidine” European Journal of Organic Chemistry 7867-7871 (2013)
Szawkało J., Maurin J.K., Pluciński F., Czarnocki Z., „Synthesis and dynamic stereochemistry of 4-aryl-thiomorpholine-3,5-dione derivatives” J Mol Struct 1079, 383-390 (2015)